Características generales de la paciente


Análisis de la historia clínica

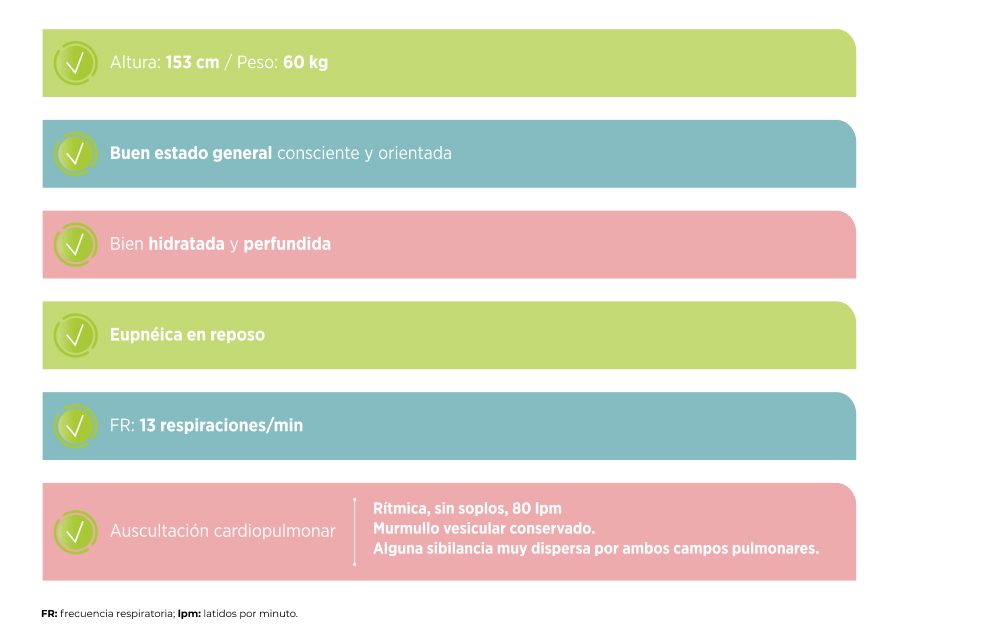
Resultados de la exploración inicial de la paciente
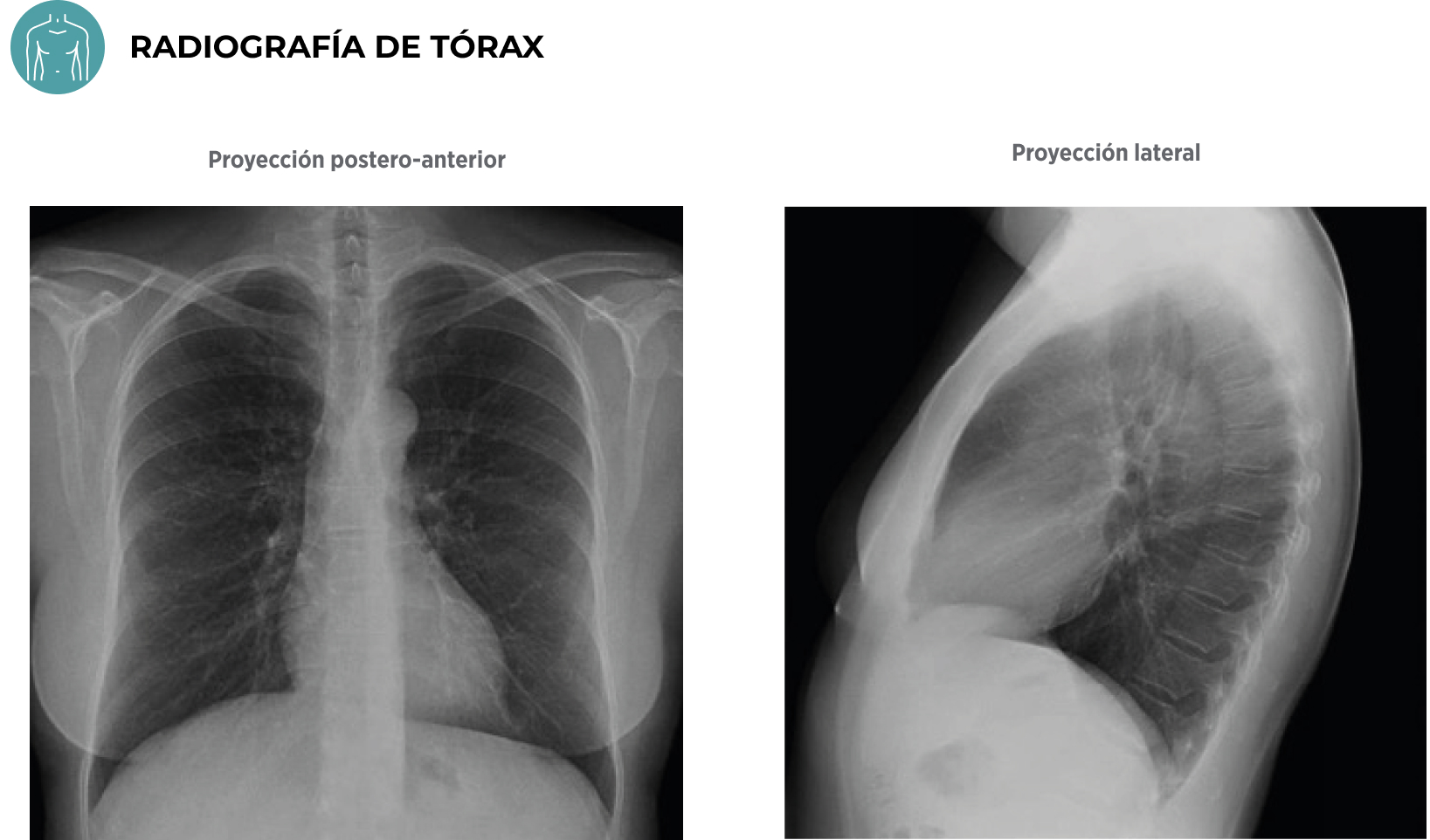
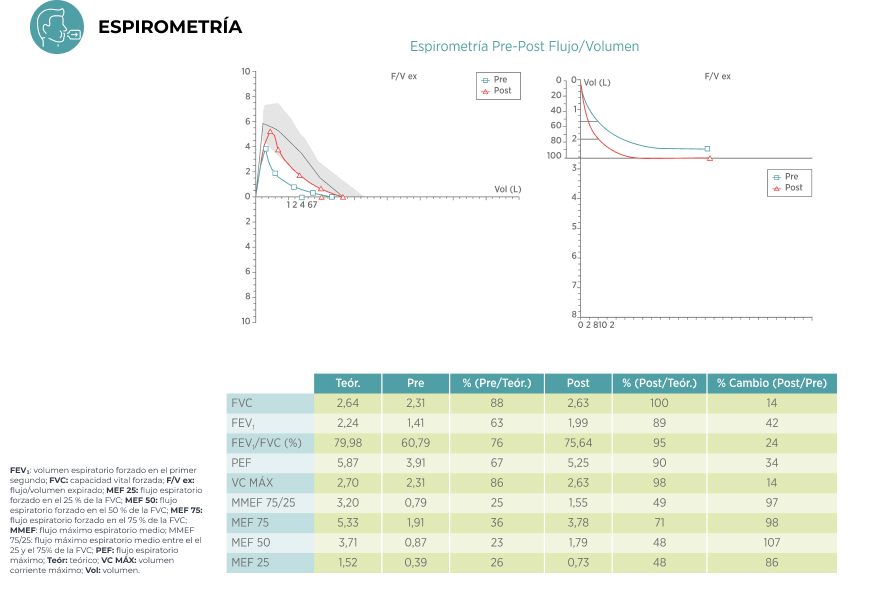
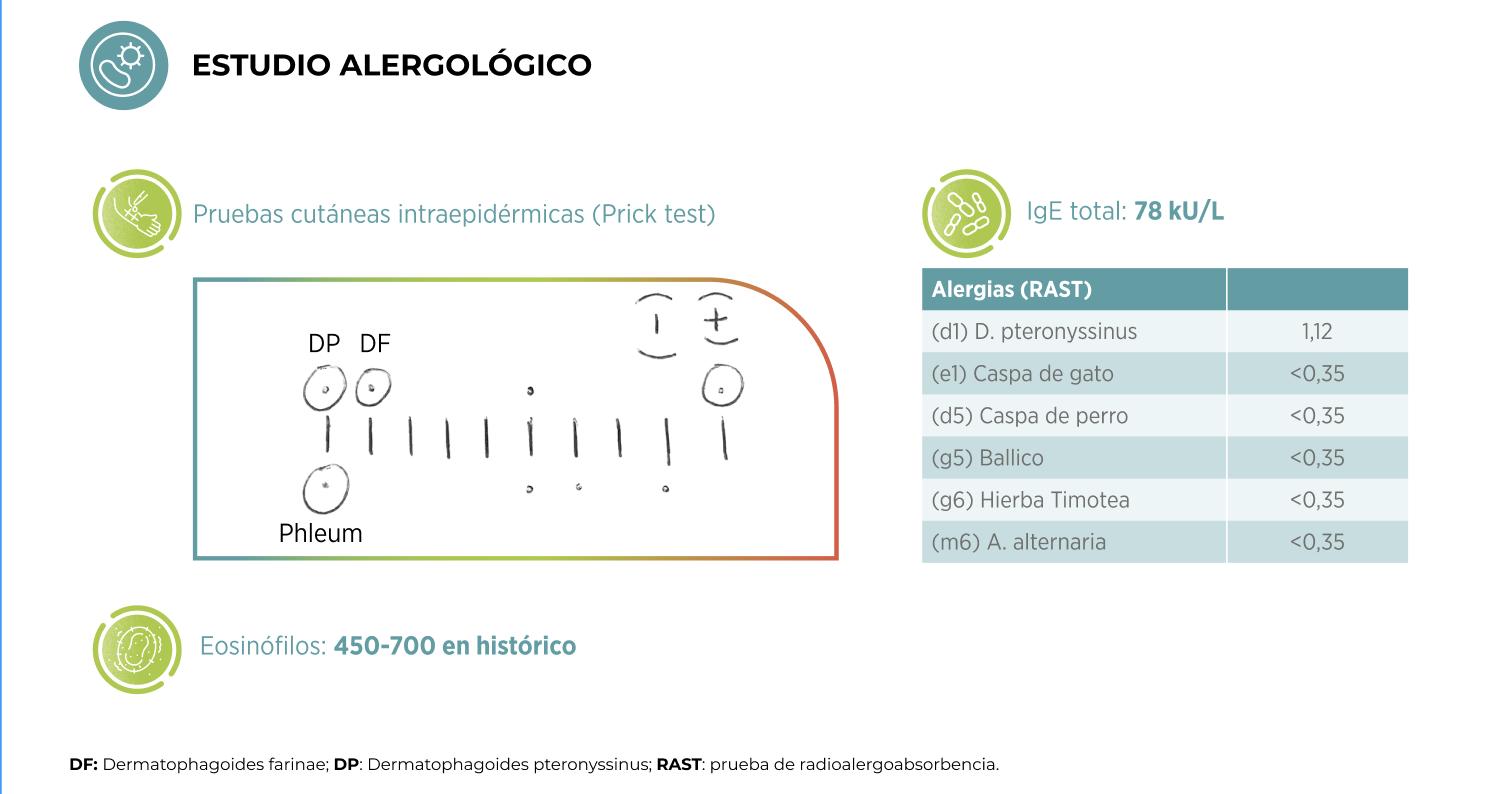
Resultados de las pruebas complementarias

¿Cuál es el diagnóstico de la paciente?

¿Qué cambio se propone en el tratamiento de la paciente?

Evolución de la paciente a los 2 meses

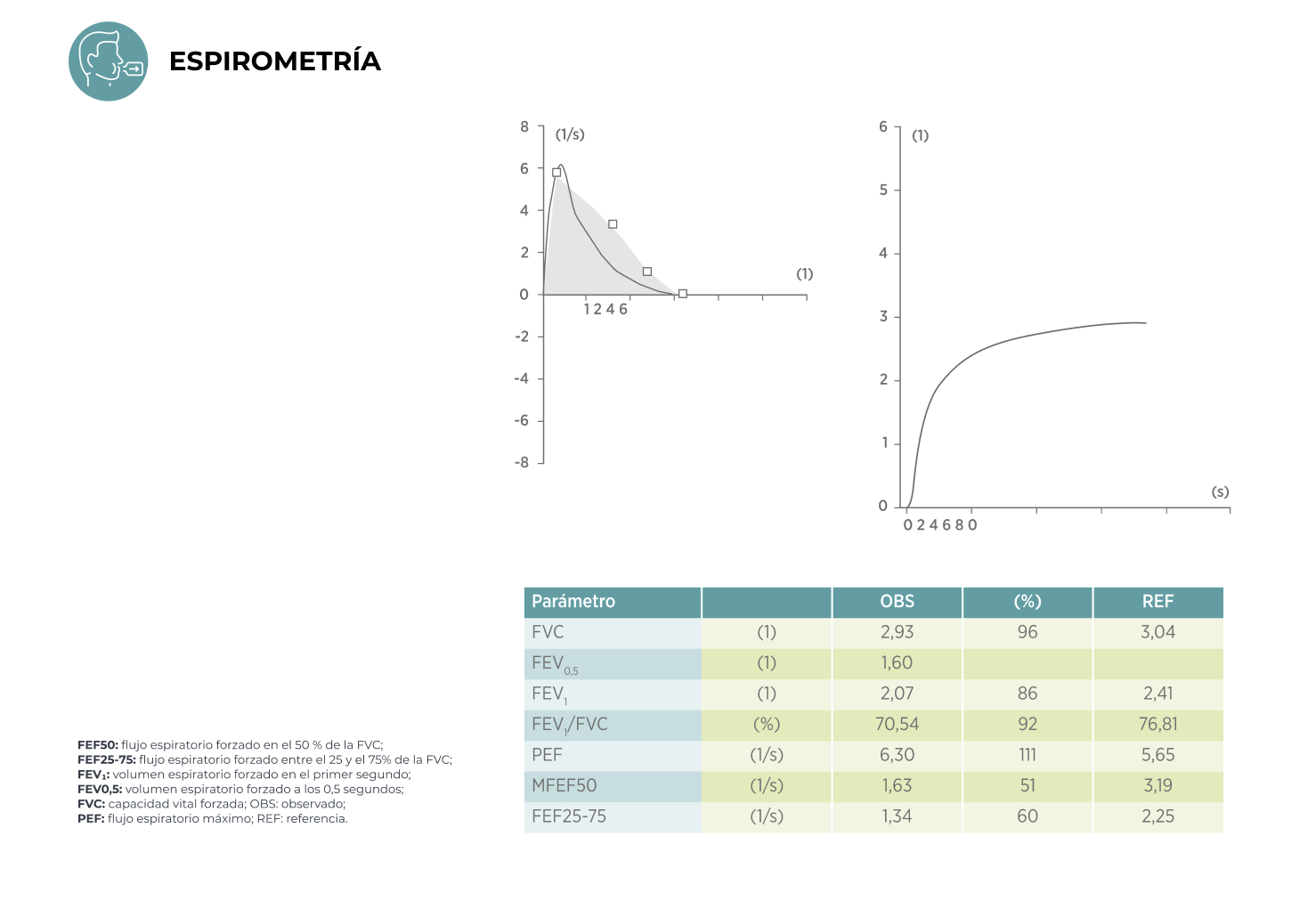
Evolución de la paciente a los 4 meses
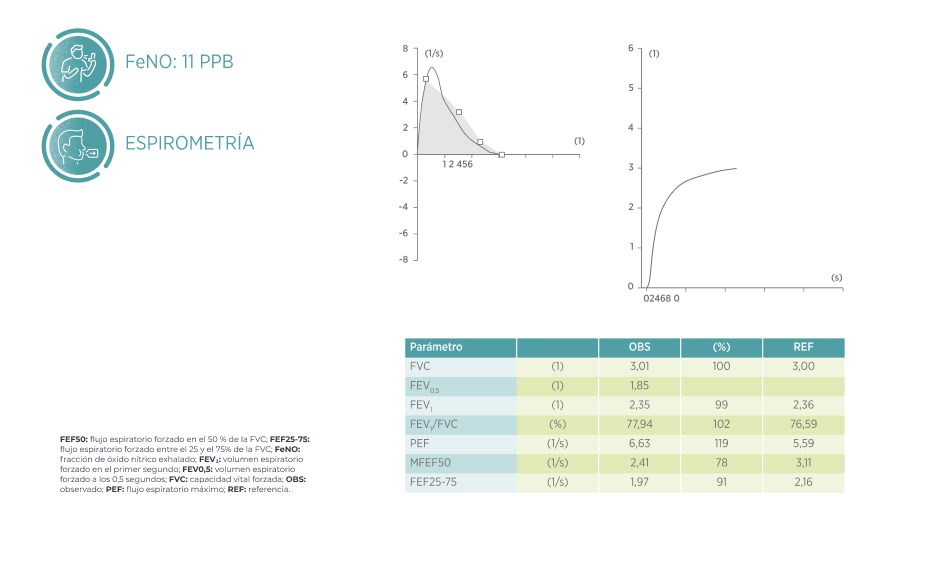
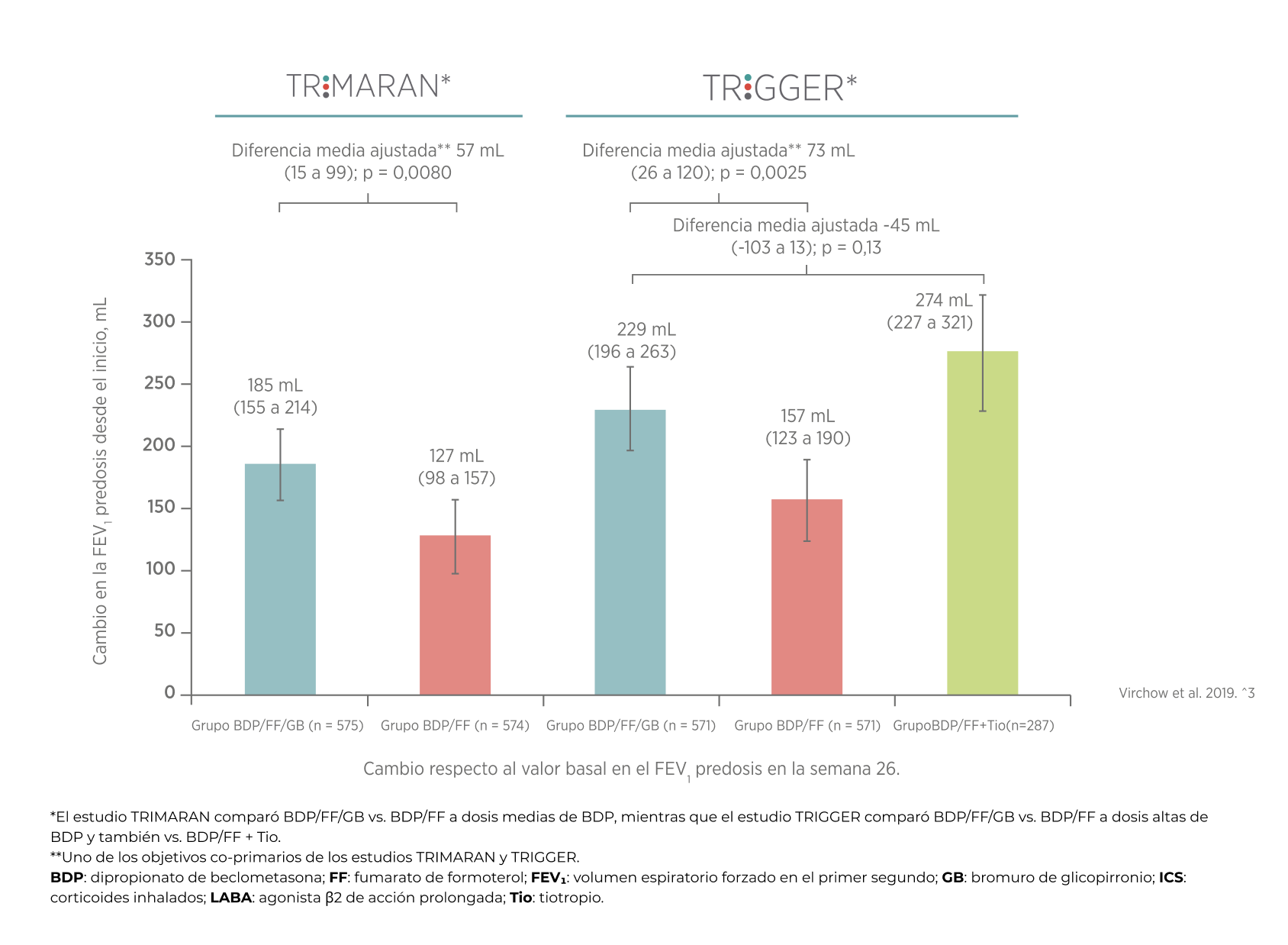
Trimbow® 172/5/9 μg mejora la función pulmonar en pacientes con asma no controlado con ICS + LABA³

Trimbow® 172/5/9 μg ha demostrado ser beneficioso en pacientes con limitación del flujo aéreo (PAL)⁴

Factores determinantes de la respuesta a la triple terapia extrafina⁵

Profundizando en la relevancia de disfunción de la pequeña vía aérea en asma⁶

Conclusiones

Ficha Técnica Trimbow® 172/5/9 μg. Consultar en: https://cima.aemps.es/cima/dochtml/ft/1171208007/FT_1171208007.html
Medicamento sujeto a prescripción médica. Reembolsable por el Sistema Nacional de Salud:
Aportación reducida (cícero). Trimbow® 172 microgramos/5 microgramos/9 microgramos solución para inhalación en envase a presión, envase conteniendo 120 dosis. PVL: 46,56€ Material revisado Marzo 2022.
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
Referencias
1. Soler X, Holbrook JT, Gerald LB, et al. Validity of the Asthma Control Test Questionnaire Among Smoking Asthmatics. J Allergy Clin Immunol Pract. 2018;6(1):151-8.
2. Guía Española para el Manejo del Asma. GEMA 5.3. Último acceso: abr 2024. Disponible en: https://www.separ.es/node/1827.
3. Virchow JC, Kuna P, Paggiaro P, et al. Single inhaler extrafine triple therapy in uncontrolled asthma (TRIMARAN and TRIGGER): two double-blind, parallel-group, randomised, controlled phase 3 trials. Lancet. 2019;394(10210):1737-49.
4. Singh D, Virchow JC, Canonica GW, et al. Extrafine triple therapy in patients with asthma and persistent airflow limitation. Eur Respir J. 2020;56(3).
5. Singh D, Virchow JC, Canonica GW, et al. Determinants of response to inhaled extrafine triple therapy in asthma: analyses of TRIMARAN and TRIGGER. Respir Res. 2020;21(1):285.
6. Postma DS, Brightling C, Baldi S, et al. Exploring the relevance and extent of small airways dysfunction in asthma (ATLANTIS): baseline data from a prospective cohort study. Lancet Respir Med. 2019;7(5):402-16.
7. Kraft M, Richardson M, Hallmark B, et al. The role of small airway dysfunction in asthma control and exacerbations: a longitudinal, observational analysis using data from the ATLANTIS study. Lancet Respir Med. 2022;10(7):661-8.
ESBCN-PRD_HCP-4483 Agosto 2024





